【平成28年(ワ)3月3日(東京地裁判決平成27年(ワ)第12416号)特許権侵害差止請求事件】
【キーワード】
包含、添加、特許法70条1項、70条2項、再現試験、再現実験、追試、広義の刊行物記載発明
第1 はじめに
本件は、オキサリプラチン溶液組成物等に関する特許権に基づき、特許権者であるスイス法人が、後発医薬品メーカーに対して、オキサリプラチン製剤の製造販売の差止め等を求めた事案である。オキサリプラチンについては、本件特許の特許権者からオキサリプラチンの日本国内における独占販売権を与えられたメーカーが、2014年2月に、「[謹告]オキサリプラチンに関する特許権について」と題された警告を広告等により発したことが話題になった(なお、本件特許は、上記警告に含まれていない。)。
本件は、医薬品の基本特許が切れた後に、組成物特許によって後発医薬品の製造販売をストップすることができた例として、医薬品のライフサイクルマネジメント上、参考となる事例である。
また、化学分野においては、先行文献に基づく新規性欠如の無効理由を構築する際に、先行文献の実施例を再現することがよく行われるが、本件は、このような再現試験の“正確性”について、裁判所では厳しく判断されることが確認された点でも参考となる。
第2 事案
1 概要
本件は、発明の名称を「オキサリプラチン溶液組成物ならびにその製造方法及び使用」とする特許第4430229号の特許権者である原告が、被告に対し、被告によるオキサリプラチン製剤の生産等が特許権侵害に当たると主張して、被告製品の生産等の差止め及び廃棄を求めた事案である。原告は、平成26年12月2日付で、本件特許に係る無効審判において、訂正請求をした(以下、訂正後の請求項1に係る発明を「本件訂正発明」という。)。訂正請求については、これを認める旨の審決が平成27年7月14日付で出されているが、当該審決は本件口頭弁論終結時において確定していない。
なお、本件原告は、本件被告以外の12社についても、本件と同様の請求をして訴訟を提起している。
2 訂正後の本件特許の請求項1記載の発明
オキサリプラチン、有効安定化量の緩衝剤および製薬上許容可能な担体を包含する安定オキサリプラチン溶液組成物であって、製薬上許容可能な担体が水であり、緩衝剤がシュウ酸またはそのアルカリ金属塩であり、
1)緩衝剤の量が、以下の:
(a)5×10-5M~1×10-2M、
(b)5×10-5M~5×10-3M、
(c)5×10-5M~2×10-3M
(d)1×10-4M~2×10-3M、または
(e)1×10-4M~5×10-4M
の範囲のモル濃度である、pHが3~4.5の範囲の組成物、あるいは
2)緩衝剤の量が、5×10-5M~1×10-4Mの範囲のモル濃度である、組成物。
第3 主な争点
1(充足論) 被告製品は、シュウ酸を添加していない(下記平衡反応式のように、オキサリプラチンを水に溶解すると、一部がジアクオDACHプラチンとシュウ酸に乖離することによってシュウ酸が自然に生ずる。)ところ、本件訂正発明において、緩衝剤たるシュウ酸は、外部から添加されたものに限定されるか否か。添加されたものに限られるのであれば、被告製品は本件訂正発明の構成要件を充足しないことになる。
2(無効論) 被告による乙1の1公報、乙6文献記載の実施例の再現試験は、乙1の1公報、乙6文献の正確な再現試験といえるか否か。正確な再現試験といえるのであれば、本件訂正発明は、乙1の1公報または乙6文献に実質的に記載されたものとして新規性がないことになる。
[平衡反応式]
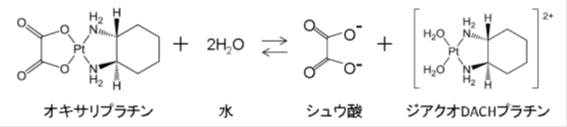
第4 判旨
「第3 当裁判所の判断
1 争点(1)ア(「(有効安定化量の)緩衝剤」(構成要件B,F,G)の充足性)について
前記前提事実(3)イのとおり、被告製品は構成要件Gに規定されているモル濃度の範囲内にある量のシュウ酸を含有するところ,このシュウ酸は添加されたものではない。原告は,「緩衝剤」であるシュウ酸はオキサリプラチン水溶液中に存在すれば足り,添加されたシュウ酸に限定されないから,被告製品は構成要件B,F及びGを充足すると主張するのに対し,被告は,「緩衝剤」であるシュウ酸はオキサリプラチン水溶液に添加されたものに限定されるから,被告製品は上記各構成要件を充足しないと主張するので,以下検討する。
(1)まず,特許請求の範囲の記載をみるに,本件発明は,その文言上,オキサリプラチン,水及び「有効安定化量の緩衝剤」である「シュウ酸またはそのアルカリ金属塩」を「包含」する「安定オキサリプラチン溶液組成物」に係る物の発明であり,緩衝剤であるシュウ酸等のモル濃度を一定の範囲に限定したものである。そして,オキサリプラチン水溶液に「包含」される緩衝剤であるシュウ酸等の量のみが規定され(構成要件G),シュウ酸等を添加することなど上記組成物の製造方法に関する記載はない。この「包含」とは「要素や事情を中にふくみもつこと」(広辞苑〔第六版〕参照)をいうことからすれば,オキサリプラチン水溶液に「包含」されるシュウ酸とは,オキサリプラチン水溶液中に存在する全てのシュウ酸をいい,添加したシュウ酸に限定されるものではないと解するのが相当である。
(2)緩衝剤であるシュウ酸に関する上記解釈は,以下のとおり,本件明細書の記載から裏付けることができる。
ア 本件明細書(甲2)の発明の詳細な説明欄には,以下の記載がある。
・・・・・・・・・・
イ 本件明細書の上記各記載を総合すると,本件発明は,従来からある凍結乾燥粉末形態のオキサリプラチン生成物及びオキサリプラチン水溶液(乙1発明)の欠点を克服し,すぐに使える形態の製薬上安定であるオキサリプラチン溶液組成物を提供することを目的とする発明であって(段落【0010】,【0012】~【0017】),オキサリプラチン,有効安定化量の緩衝剤及び製薬上許容可能な担体を包含する安定オキサリプラチン溶液組成物に関するものである(同【0018】)。この緩衝剤は本件発明の組成物中に存在することでジアクオDACHプラチン等の不純物の生成を防止し,又は遅延させ得ることができ(同【0022】,【0023】),これによって本件発明はこれら従来既知のオキサリプラチン組成物と比較して優れた効果,すなわち,①凍結乾燥粉末形態のオキサリプラチン生成物と比較すると,低コストであって複雑でない製造方法により製造が可能であること,投与前の再構築を必要としないので再構築に際してのミスが生じることがないこと,②従来既知の水性組成物(乙1)と比較すると,製造工程中に安定であること(ジアクオDACHプラチンやジアクオDACHプラチン二量体といった不純物が少ないこと)といった効果を有するもの(同【0030】,【0031】)と認められる。そうすると,本件明細書の記載からは,本件発明が,従来既知のオキサリプラチン組成物(凍結乾燥粉末形態のものや乙1発明のように水溶液となっているもの)の欠点を克服し,改良することを目的とし,その解決手段としてシュウ酸等を緩衝剤として包含するという構成を採用したと認められるのであり,更にこの緩衝剤を添加したものに限定するという構成を採用したとみることはできない。
(3)以上によれば,構成要件Gに規定されたモル濃度の範囲内にある量のシュウ酸を含んでいれば構成要件B,F及びGを充足すると解すべきところ,被告製品は前記前提事実(3)イのとおりこれを含有する。したがって、被告製品は本件発明の技術的範囲に属すると判断するのが相当である。
3 争点(2)ア(乙1発明又は乙6発明に基づく新規性欠如)について
(1)乙1発明に基づく新規性欠如
ア 本件特許の優先日前に頒布された刊行物である乙1の1公報には,以下の記載がある(以下では,乙1の2公報の請求項及び頁番号を引用する。)。
なお,「オキサリプラティヌム」と「オキサリプラチン」は同義である。
・・・・・・・・・・
(エ)「実施例1:オキサリプラティヌム水溶液の製造
ガラスまたはステンレス製の恒温容器中に,必要量の約80%の注射用水を入れ,この水を攪拌(800-1200rpm)下40℃±5℃に加温する。例えば2mg/mlの濃度とするに必要な量のオキサリプラティヌムを別に秤量し,加温した水に加える。秤量用容器を注射用水で3回洗浄し,これを混合物に加える。混合物をさらに上記温度で30±5分間または必要ならそれ以上,オキサリプラティヌムが完全に溶けるまで攪拌する。一つの変法では,酸素含量を減少させるため水に窒素を吹き込むことができる。
次いで,溶液に注射用水を加えて目的容量または重量に調整し,さらに10±2分間(800-1200rpm)ホモジネートし,最後に攪拌しながら約30℃に冷却する。この段階で,通常の試験を実施するため溶液の試料を取り,対照と溶液をそれ自体公知の方法により無菌濾過して澄明な溶液とし,この溶液は充填前には15-30℃で貯蔵する。」(6頁1~13行)
(オ) 「実施例2:容器充填
次に,例えば2mg/mlの濃度のオキサリプラティヌム水溶液を,好ましくは不活性雰囲気,例えば窒素中で,滅菌した発熱物質無含有の50mlガラスバイアル中に,無菌的に充填する。」(6頁17~20行)
(カ) 「実施例3:安定性試験前記のようにして得られ,種々の容器中,具体的には2種の異なる栓,すなわち:
栓A:「オムニフレックス」
栓A(N):同(上部空間にN2充填)
栓B:「グレイブチル」(同上)
を用いて貯蔵したオキサリプラティヌム水溶液について,経時的に安定性試験を実施した。」(7頁1~8行)
「使用した分析法は,当業界で現在使用されているものの一つ,すなわち,例えばザ・ジャーナル・オブ・パレンテラル・ドラッグ・アソシエーション108-109頁,1979年に記載されているような,高速液体クロマトグラフィー(HPLC)である。クロマトグラムのピーク分析は,不純物の含量と百分率の測定を可能にし,そのうち主要なものは蓚酸であると同定した。」(7頁13~17行)
(サ)「 得られた結果は,下記の表に要約する。」(7頁19行)
・・・・・・・・・・
エ これに対し,被告は,①乙1の1公報の追試結果(乙5,14)によれば,乙1発明におけるシュウ酸のモル濃度は6.07×10-5~7.54×10-5Mの範囲に,②乙1の1公報の実施例におけるシュウ酸のモル濃度を試算すると,5.35×10-5~5.61×10-5Mの範囲にあり,いずれも構成要件Gが規定するモル濃度の範囲内であるから,上記ウの点は相違点とはならない旨主張する。
そこで判断するに,①については,乙1発明においてはその特許請求の範囲の記載からしてpHの値がオキサリプラチン水溶液の安定性,すなわち不純物(これにはシュウ酸も含まれる。)の量に影響する重要な要素の一つであると考えられるところ ),乙1の1公報の実施例におけるpHの値は5.29~5.65の範囲にあるのに対し(乙1の2公報の8頁の表),上記追試においては5.8~6.1(乙5)又は5.7~6.6(乙14)の範囲にある。このことからすれば,被告のいう追試は,乙1の1公報を正確に再現したものとみることはできないから,これらが正確な追試であることを前提とする被告の上記主張①は採用することができない。
②については,被告は,乙1の1公報の実施例における「不純物」(乙1の2公報の8頁の表)の数値を基に,オキサリプラチンの分解により発生する不純物がシュウ酸及びジアクオDACHプラチン又はジアクオDACHプラチン二量体のみであると仮定して,シュウ酸のモル濃度を試算している。しかし,乙1の1公報には上記「不純物」について「クロマトグラムのピークの分析は,不純物の含量と百分率の測定を可能にし,そのうち主要なものは蓚酸であると同定した。 )との説明があるのみで,その具体的な内容について言及がないから,上記「不純物」をシュウ酸とジアクオDACHプラチン又はジアクオDACHプラチン二量体のみとする仮定は正確でないというべきである。したがって,被告の上記主張②も採用することができない。
(2) 乙6発明に基づく新規性欠如
・・・・・・・・・・
ウ これに対し,被告は,乙6文献の追試結果(乙7)によれば,乙6発明におけるシュウ酸のモル濃度は7.49×10-5Mであり,構成要件Gが規定するモル濃度の範囲内であるから,上記アの点は相違点とはならない旨主張する。
そこで判断するに,上記追試では,7.5mg/mlの濃度のオキサリプラチン水溶液を分析対象とし,その水溶液中のシュウ酸のモル濃度を測定している。しかし,乙6文献においては溶解度が7.9mg/mlのオキサリプラチンが開示されているのみであり(乙6文献の916頁3行),オキサリプラチン水溶液の濃度が開示されているわけではないから,上記の追試が乙6文献を正確に再現したものみることはできない。したがって,この点についても被告の主張を採用することができない。」
第4 検討
1 添加と包含について
組成物発明に関する特許権の侵害が問題となる場合、特許発明の構成要件に係る成分が、他の成分の不純物として含まれていたり、被疑侵害製品内での自然な反応によって生じたりして、意図して添加しなくとも被疑侵害製品に含まれてしまうことがある。このような場合、特許請求の範囲及び明細書の記載から、特許発明において、ある成分が「添加される」ものなのか、「包含される」ものなのかを解釈することになる(特許法70条1項、70条2項)。
本件訂正発明の構成要件に係るシュウ酸は、上記平衡反応式で示したように、オキサリプラチンを水に溶かすとオキサリプラチンが解離してシュウ酸が生ずるため、オキサリプラチンの水溶液中に不可避的に含まれるものである。被告は、被告製品に外部からシュウ酸を添加していないものの、被告製品中のシュウ酸の含有量が本件訂正発明の規定範囲内であった。被告は、縷々主張して、本件訂正発明において、緩衝剤であるシュウ酸は、添加したシュウ酸を意味するとして争ったが、裁判所は、特許請求の範囲の文言上、「包含する」となっていること、本件特許明細書をみても、シュウ酸を添加したものに限定しているとみることはできないとし、シュウ酸が本件訂正発明の規定量含まれていれば、添加されたものかどうかにかかわらず、本件訂正発明の構成要件を充足すると判断した。
2 再現試験(追試)について
化学分野における数値限定発明に関する特許については、特許発明が、既に存在していた物質について数値限定を加えただけで見かけ上は新規性があるが、実際上は、昔から知られていたものと何ら変わりがないように思われるケースがある。このようなケースでは、特許発明に係る数値限定そのものずばりを開示した文献が見つからないことが意外に多く、特許権の侵害警告を受けた側や特許権侵害訴訟の被告にしてみると、昔から知られていたはずなのにその特許を無効にすることができないという歯痒い思いをすることがある。
この点について、平成26年9月25日知財高裁判決(平成26年(ネ)第10018号)は、対象の特許発明の構成の相当部分が先行文献に記載され、その特許発明の一部の構成(結晶構造等の属性)が明示的には記載されていないときに、当業者が、当該先行文献記載の実施例を再現実験して当該物質を作成し、その構成(結晶構造等の属性)を確認し得るときには、先行文献中の明示的な記載と、再現実験により確認される属性とを含めて「刊行物に記載された発明」と評価できると判示した(「広義の刊行物記載発明」)。
この判示内容に従えば、数値限定を含む組成物発明について、先行文献に組成物の構成成分が開示され、数値限定だけ開示がないケースでも、その先行文献記載の実施例を再現して組成物を製造し、その再現した組成物を測定にかけた結果、特許発明にかかる数値範囲を充足すれば、当該特許発明は、実質的に先行文献に記載されているとして新規性が否定されることになる。
ところが、この再現試験の正確性が争いとなる。特許文献や学術論文中の組成物の製造方法は必要最低限の記載しかないことが多く、先行文献の実施例に記載されていない製造条件や操作については技術常識等で埋めることになる。この点、特許権者側からすると、被告による再現試験は、被告による恣意的な条件設定、操作が含まれており、先行文献の実施例の正確な再現とはいえないということになる。
本件では、被告が乙1の1公報及び乙6文献のそれぞれについて実施例を追試し、シュウ酸の濃度が本件訂正発明の構成要件の範囲内になると主張したが、裁判所は、被告による再現試験は、乙1の1公報及び乙6文献のそれぞれの正確な再現ではないとして、被告の主張は採用せず、本件訂正発明は、新規性(進歩性も)があるとした。これは、再現試験の正確性について厳しい判断であるといえる。
乙6文献の再現試験については、乙6文献には、最も重要である主成分のオキサリプラチンの濃度が開示されていないことから、乙6文献をベースに広義の刊行物記載発明の論理構成をすること自体が当初から困難であったと思われる。
一方、乙1の1公報については、上記のように製造方法がかなり具体的に開示されており、被告の方ではこの具体的に記載された方法をトレースしたものと考えられるのに、本件判決では、被告の再現試験の方法については特に触れず、結果として得られた組成物のpH(pH5.8~6.1ないし5.7~6.6)が乙1の1(pH5.29~5.65)とは異なるとして、再現試験の正確性を否定している。この点、pHは、測定装置や測定時の温度、校正などによって、測定結果の変動が大きく、たとえpHの値がオキサリプラチン水溶液中のシュウ酸の量に与える影響が大きいとしても、pHの値の違いだけで再現試験の正確性を判断することについては一考の余地がありそうである。
(文責)弁護士 篠田 淳郎


