【平成28年2月16日判決(東京地裁 平成26年(ワ)第17390号)】
【判旨】
発明の名称を「ヘリコバクター・ピロリへの感染を判定する検査方法及び検査試薬」とする特許権(特許第3504633号)を有する原告が,被告に対し,被告による被告製品1及び2の輸入等が特許権侵害に当たると主張して,それらの輸入等の差止め及び廃棄並びに損害賠償を求めた事案において,被告製品1及び2のモノクローナル抗体は,ヘリコバクター・ピロリのネイティブなカタラーゼだけでなく,変性剤で変性されたカタラーゼとも結合するモノクローナル抗体であるから,構成要件1Bの「ヘリコバクター・ピロリのネイティブなカタラーゼに対するモノクローナル抗体」に当たらず,したがって,被告製品1及び2が構成要件1Bを充足すると認めることはできないなどとして,請求を棄却した事例。
【キーワード】
特許法第70条第1項,特許法第70条第2項
1 特許発明の内容
本件特許権の請求項6に係る発明(以下「本件特許発明」という。)の内容は,以下のとおりである。
| 構成要件 |
内容 |
| 1A | 消化管排泄物中に存在するヘリコバクター・ピロリのネイティブなカタラーゼを検出することにより,ヘリコバクター・ピロリへの感染を判定するための試薬であって, |
| 1B | ヘリコバクター・ピロリのネイティブなカタラーゼに対するモノクローナル抗体を構成成分とする |
| 1C | ことを特徴とする検査試薬。 |
ヘリコバクター・ピロリ(Helicobacter pylori)とは,ヒトの胃粘膜に見られる細菌であり,胃潰瘍、十二指腸潰瘍、慢性胃炎、更には胃癌等のさまざまな胃、十二指腸疾患の原因となりうるもので,先進国,特に日本での感染率が非常に高い(40歳以上では80%)ことから問題となっている。とされている。しかし,ヘリコバクター・ピロリ感染を,非侵襲的な方法で且つ精度良く検出することが難しく,その点が課題となっていた。
本発明は,従来は消化管中でタンパク質分解酵素により分解されてしまうと考えられていた,ヘリコバクター・ピロリのネイティブなカタラーゼが,ヘリコバクター・ピロリ感染者の糞便中に残存しているとの発見に基づき,当該カタラーゼを感染判定のための指標として検出する試薬である。
2 争点(構成要件1Bの充足性)
被告は,構成要件1Bにおける「ヘリコバクター・ピロリのネイティブなカタラーゼに対するモノクローナル抗体」とは,ヘリコバクター・ピロリ由来のカタラーゼのうちネイティブなカタラーゼのみと結合するモノクローナル抗体を意味し,それ以外のカタラーゼ(例えば,SDS等の変性剤によって変性されたカタラーゼ)とも結合可能なモノクローナル抗体はこれに含まれないと主張した(クレーム解釈)。
そして,被告製品1は,「ELISA法(酵素免疫測定法)による糞便中のヘリコバクター・ピロリ抗原検出用試薬」であり,被告製品2は,「免疫クロマト法による糞便中のヘリコバクター・ピロリ抗原検出用試薬」であるところ,それぞれヘリコバクター・ピロリのネイティブなカタラーゼの他に,SDS等の変性剤によって変性されたヘリコバクター・ピロリのカタラーゼとも結合可能なものであるから,被告製品1乃至2は構成要件1Bを充足しないと主張した(あてはめ)。
よって,本件の主な争点は下記の2点である。
(1)「ヘリコバクター・ピロリのネイティブなカタラーゼに対するモノクローナル抗体」とは,SDS等の変性剤によって変性されたヘリコバクター・ピロリのカタラーゼとも結合可能なモノクローナル抗体を含むか否か(クレーム解釈)
(2)被告製品1乃至2は,SDS等の変性剤によって変性されたヘリコバクター・ピロリのカタラーゼと結合可能か否か

3 裁判所の判断
(1)争点1(クレーム解釈)について
まず,裁判所は,特許法70条1項に基づくクレーム解釈について,クレーム文言のみからでは,構成要件1Bのモノクローナル抗体の意義が明らかでないとした(下記参照)。
次に,裁判所は,明細書の記載のうち従来の技術・発明が解決しようとする課題・課題を解決するための手段・実施例・発明の効果の各項目の記載を引用しつつ,本件特許発明の技術的意義について次のように認定した(下記参照)。
そして,裁判所は,構成要件1Bの解釈について,下記のとおり,SDS等の変性剤で変性されたカタラーゼと結合可能なモノクローナル抗体は含まれないと結論付けた(下記参照)。
なお,裁判所は,原告の出願経過における主張についても,下記のとおり上記の解釈を裏付けるものとして引用・認定している。
(2)争点2(あてはめ)について
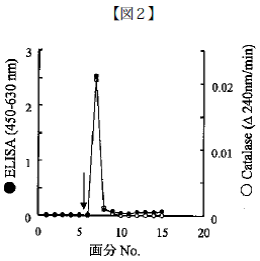
被告は,被告製品1乃至2に用いられているモノクローナル抗体について,SDS及び2ME(メルカプトエタノール)による変性処理並びに煮沸処理を経たカタラーゼを検出するとの実験結果を提出した。一方,原告は,上記の変性処理及び煮沸処理を経たカタラーゼを検出しないとの実験結果を提出し,両者の主張は真っ向から対立した。
この点について,裁判所は,下記のとおり判断した。
・・・(中略)・・・
同③については,原告による実験(甲7,14)においてはいずれもSDS及び2MEによる変性処理並びに煮沸処理により変性したカタラーゼが検出されなかったことが認められる。しかし,これらの実験で試料として用いられたのは被告製品1及び2であって,被告による前記実験(乙26,34)で用いられた被告製品1及び2のモノクローナル抗体ではない。そして,被告製品1及び2の測定原理(固相抗体と標識抗体で抗原(カタラーゼ)を挟み込むことにより抗原を検出すること。甲3,5,乙27,弁論の全趣旨)に照らすと,カタラーゼが完全に変性して単量体となっている場合には固相抗体と標識抗体の一方しかこのカタラーゼと結合することができないため,被告製品1及び2は完全に変性したカタラーゼを検出できないと考えられることを踏まえれば,原告による上記実験において被告製品1及び2が完全に変性したカタラーゼを検出しなかったとしても,このことから直ちに被告製品1及び2で用いられているモノクローナル抗体が変性したカタラーゼと結合したとする被告による前記実験結果の信用性が害されることはないというべきである。したがって,原告の上記主張③は前記オの判断に影響するものでないと解される。
そして,下記のとおり,被告製品1乃至2は構成要件1Bを充足しないと結論付けた。
4 検討
(1)クレーム解釈(争点1)について
裁判所が認定した本件明細書の記載のうち,【0011】には,本件明細書の「カタラーゼ」が,SDS等の変性剤で変性,乖離されたカタラーゼを含まない旨の記載がある(下記参照)。この部分の記載は,構成要件1Bのクレーム解釈において,非常に重要なウエイトを占めたのではないかと推察される。

また,本件特許発明の課題及び作用効果(=ヘリコバクター・ピロリの検出精度を高める)の観点からも,変性カタラーゼを同時に検出可能なモノクローナル抗体では,特異性が低下してしまい上記の作用効果を十分に達成できないと考えられることから,構成要件1Bの解釈において,「ネイティブなカタラーゼのみと結合するモノクローナル抗体であって,SDS等の変性剤で変性されたカタラーゼとは結合しないものをいう」とすることは合理的である。
加えて,原告自身が,従来技術との差別化のために,本件特許発明のモノクローナル抗体が「SDSにより変性されたカタラーゼとは結合することができないものである」とわざわざ限定した説明を行っている点に鑑みると,裁判所のクレーム解釈は,本件特許発明の本質(課題・解決手段・作用効果)を捉えた妥当なものであると考えられる。
(2)あてはめ(争点2)について
原告と被告の実験結果をまとめると,下記のとおりであった(「変性カタラーゼの検出」が「×」の場合,構成要件1B充足可能性あり)。
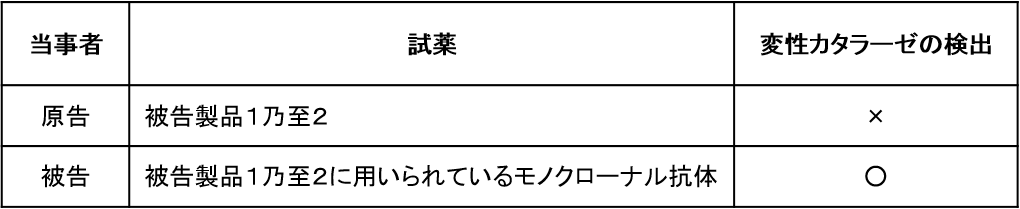
ここで,本件特許発明の構成要件1Bは,「・・・カタラーゼに対する検査試薬を構成成分とする」ではなく,「・・・カタラーゼに対するモノクローナル抗体を構成成分とする」と記載されていることからすれば,構成要件充足性を判断するための実験としては,被告製品そのものではなく,製品中に含まれるモノクローナル抗体を用いることが合理的である。
よって,被告の実験結果を採用した裁判所の判断は妥当であったと考えられる。
(3)実務上の指針
本判決は,明細書の各項目の記載に基づき発明の技術的意義を認定し,当該認定に沿ったクレーム解釈・あてはめを行うという,構成要件充足性の典型的な判断手法を示したものといえ,充足性判断の具体例として,技術分野を問わず広く参考になると考えられる。
以上
(文責)弁護士・弁理士 丸山真幸


