【知財高裁大合議平成30年4月13日判決(平成28年(行ケ)10182号)】
【キーワード】大合議、進歩性、訴えの利益
【判旨】医薬発明の進歩性が争われた大合議事件である。原告日本ケミファが、被告塩野義製薬株式会社のピリミジン誘導体特許に対して無効審判を申し立てた事件の取消訴訟である。知財高裁特別部は、「当該刊行物に化合物が一般式の形式で記載され,当該一般式が膨大な数の選択肢を有する場合には,当業者は,特定の選択肢に係る具体的な技術的思想を積極的あるいは優先的に選択すべき事情がない限り,当該刊行物の記載から当該特定の選択肢に係る具体的な技術的思想を抽出することはできない」との判断を示した。
1.本件特許
特許第2648897号
ピリミジン誘導体(HMG-CoAレダクターゼと呼ばれるコレステロール降下剤。「スタチン」として知られる)
特許権者:塩野義製薬株式会社
優先日:平成3年(1991年)7月1日
出願日:平成4年(1992年)5月28日
登録日:平成9年(1997年)5月16日
権利消滅日:平成29年(2017年)5月28日
無効審判1:テバ製薬(平成26年2月4日請求、一部無効)
無効審判2(本件第2事件):日比野謙一(平成27年3月31日請求、一部無効)
無効審判3(本件第1事件):日本ケミファ(平成28年3月9日、一部無効)
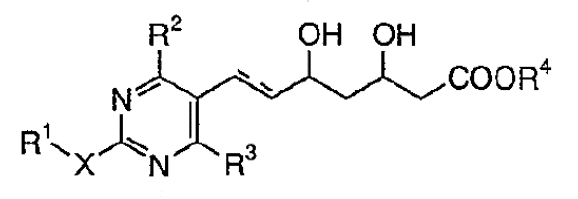
【請求項1】(本件発明1)
式(I):
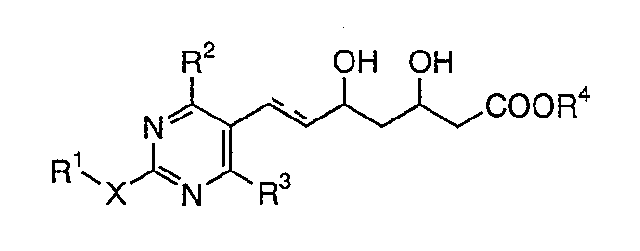
【化1】
(式中,
R1は低級アルキル;
R2はハロゲンにより置換されたフェニル;
R3は低級アルキル;
R4は水素またはヘミカルシウム塩を形成するカルシウムイオン;
Xはアルキルスルホニル基により置換されたイミノ基;
破線は2重結合の有無を,それぞれ表す。)
で示される化合物またはその閉環ラクトン体である化合物。
2 判決
ア 規範
|
特許法29条1項は,「産業上利用することができる発明をした者は,次に掲げる発明を除き,その発明について特許を受けることができる。」と定め,同項3号として,「特許出願前に日本国内又は外国において」「頒布された刊行物に記載された発明」を挙げている。同条2項は,特許出願前に当業者が同条1項各号に定める発明に基づいて容易に発明をすることができたときは,その発明については,特許を受けることができない旨を規定し,いわゆる進歩性を有していない発明は特許を受けることができないことを定めている。 上記進歩性に係る要件が認められるかどうかは,特許請求の範囲に基づいて特許出願に係る発明(以下「本願発明」という。)を認定した上で,同条1項各号所定の発明と対比し,一致する点及び相違する点を認定し,相違する点が存する場合には,当業者が,出願時(又は優先権主張日。以下「3 取消事由1について」において同じ。)の技術水準に基づいて,当該相違点に対応する本願発明を容易に想到することができたかどうかを判断することとなる。 このような進歩性の判断に際し,本願発明と対比すべき同条1項各号所定の発明(以下「主引用発明」といい,後記「副引用発明」と併せて「引用発明」という。)は,通常,本願発明と技術分野が関連し,当該技術分野における当業者が検討対象とする範囲内のものから選択されるところ,同条1項3号の「刊行物に記載された発明」については,当業者が,出願時の技術水準に基づいて本願発明を容易に発明をすることができたかどうかを判断する基礎となるべきものであるから,当該刊行物の記載から抽出し得る具体的な技術的思想でなければならない。そして,当該刊行物に化合物が一般式の形式で記載され,当該一般式が膨大な数の選択肢を有する場合には,当業者は,特定の選択肢に係る具体的な技術的思想を積極的あるいは優先的に選択すべき事情がない限り,当該刊行物の記載から当該特定の選択肢に係る具体的な技術的思想を抽出することはできない。 したがって,引用発明として主張された発明が「刊行物に記載された発明」であって,当該刊行物に化合物が一般式の形式で記載され,当該一般式が膨大な数の選択肢を有する場合には,特定の選択肢に係る技術的思想を積極的あるいは優先的に選択すべき事情がない限り,当該特定の選択肢に係る具体的な技術的思想を抽出することはできず,これを引用発明と認定することはできないと認めるのが相当である。 この理は,本願発明と主引用発明との間の相違点に対応する他の同条1項3号所定の「刊行物に記載された発明」(以下「副引用発明」という。)があり,主引用発明に副引用発明を適用することにより本願発明を容易に発明をすることができたかどうかを判断する場合において,刊行物から副引用発明を認定するときも,同様である。したがって,副引用発明が「刊行物に記載された発明」であって,当該刊行物に化合物が一般式の形式で記載され,当該一般式が膨大な数の選択肢を有する場合には,特定の選択肢に係る具体的な技術的思想を積極的あるいは優先的に選択すべき事情がない限り,当該特定の選択肢に係る具体的な技術的思想を抽出することはできず,これを副引用発明と認定することはできないと認めるのが相当である。そして,上記のとおり,主引用発明に副引用発明を適用することにより本願発明を容易に発明をすることができたかどうかを判断する場合には,①主引用発明又は副引用発明の内容中の示唆,技術分野の関連性,課題や作用・機能の共通性等を総合的に考慮して,主引用発明に副引用発明を適用して本願発明に至る動機付けがあるかどうかを判断するとともに,②適用を阻害する要因の有無,予測できない顕著な効果の有無等を併せ考慮して判断することとなる。特許無効審判の審決に対する取消訴訟においては,上記①については,特許の無効を主張する者(特許拒絶査定不服審判の審決に対する取消訴訟及び特許異議の申立てに係る取消決定に対する取消訴訟においては,特許庁長官)が,上記②については,特許権者(特許拒絶査定不服審判の審決に対する取消訴訟においては,特許出願人)が,それぞれそれらがあることを基礎付ける事実を主張,立証する必要があるものということができる。 |
イ あてはめ
(ア)主引用発明の選択について
|
前記2(2)のとおり,本件発明は,コレステロール生合成の律速酵素である3-ヒドロキシ-3-メチルグルタリルコエンザイムA(HMG-CoA)還元酵素を特異的に阻害し,コレステロールの合成を抑制することにより,高コレステロール血症,高リポタンパク血症,更にはアテローム性動脈硬化症の治療に有効な,HMG-CoA還元酵素阻害剤に関するものであり,前記(2)アのとおり,甲1発明も,コレステロール生合成における律速酵素である3-ヒドロキシ-3-メチルグルタリル補酵素A(HMG-CoA)の拮抗阻害剤であって,血中コレステロールレベルを降下させる過脂肪蛋白血症処置剤及び抗アテローム性動脈硬化剤に関するものであるから,本件発明と技術分野を共通にし,本件発明の属する技術分野の当業者が検討対象とする範囲内のものであるといえる。 また,本件発明1と前記(2)イ認定の甲1発明とを対比すると,審決の認定のとおり,次の【一致点】記載の点で一致し,この点において,当事者間に争いはなく,近似する構成を有するものであるから,甲1発明は,本件発明の構成と比較し得るものであるといえる。 【一致点】 (式中, R1は低級アルキル; そうすると, 甲1発明は,本件発明の進歩性を検討するに当たっての基礎となる,公知の技術的思想といえる。 以上によると,甲1発明は,本件発明についての特許法29条2項の進歩性の判断における主引用発明とすることが不相当であるとは解されない。これに反する被告らの主張を採用することはできない。 |
(イ)対比
|
前記(イ)のとおり,甲2の一般式(I)で示される化合物は,甲1の一般式Iで示される化合物と同様,HMG-CoA還元酵素阻害剤を提供しようとするものであり,ピリミジン環を有し,そのピリミジン環の2,4,6位に置換基を有する化合物である点で共通し,甲1発明の化合物は,甲2の一般式(I)で示される化合物に包含される。 甲2には,甲2の一般式(I)で示される化合物のうちの「殊に好ましい化合物」のピリミジン環の2位の置換基R3の選択肢として「-NR4R5」が記載されるとともに,R4及びR5の選択肢として「メチル基」及び「アルキルスルホニル基」が記載されている。 しかし,甲2に記載された「殊に好ましい化合物」におけるR3の選択肢は,極めて多数であり,その数が,少なくとも2000万通り以上あることにつき,原告らは特に争っていないところ,R3として,「-NR4R5」であってR4及びR5を「メチル」及び「アルキルスルホニル」とすることは,2000万通り以上の選択肢のうちの一つになる。 また,甲2には,「殊に好ましい化合物」だけではなく,「殊に極めて好ましい化合物」が記載されているところ,そのR3の選択肢として「-NR4R5」は記載されていない。 さらに,甲2には,甲2の一般式(I)のXとAが甲1発明と同じ構造を有する化合物の実施例として,実施例8(R3はメチル),実施例15(R3はフェニル)及び実施例23(R3はフェニル)が記載されているところ,R3として「-NR4R5」を選択したものは記載されていない。 そうすると,甲2にアルキルスルホニル基が記載されているとしても,甲2の記載からは,当業者が,甲2の一般式(I)のR3として「-NR4R5」を積極的あるいは優先的に選択すべき事情を見いだすことはできず,「-NR4R5」を選択した上で,更にR4及びR5として「メチル」及び「アルキルスルホニル」を選択すべき事情を見いだすことは困難である。 したがって,甲2から,ピリミジン環の2位の基を「-N(CH3)(SO2R’)」とするという技術的思想を抽出し得ると評価することはできないのであって,甲2には,相違点(1-ⅰ)に係る構成が記載されているとはいえず,甲1発明に甲2発明を組み合わせることにより,本件発明の相違点(1-ⅰ)に係る構成とすることはできない。 |
(ウ)原告主張の排斥
|
原告らは,甲2には,一般式(Ⅰ)の化合物全体の製造方法及びHMG-CoA還元酵素阻害活性について記載されているから,「R3」として「NR4R5」を選択した一般式(Ⅰ)の化合物について技術的裏付けがあると理解できるのであって,「甲2では,「R3」として「NR4R5」を選択した化合物については,その製造方法もHMG-CoA還元酵素阻害活性の薬理試験も記載されていない」旨の審決の認定は誤りである旨主張する。 前記aのとおり,甲2の一般式(I)で示される化合物は,HMG-CoA還元酵素阻害剤を提供しようとするものであり,前記(イ)a(g)のとおり,甲2には,甲2の一般式(I)で示される化合物に包含される甲2の実施例1~23の化合物が,メビノリンと比較して高いHMG-CoA還元酵素阻害活性を有する旨が記載されている。また,甲16には甲2の一般式(Ⅰ)の範囲内の特定の化合物についてHMG-CoA還元酵素阻害活性を有することが記載されており,証拠(甲16,73~75)及び弁論の全趣旨によると,当業者は,甲2の実施例の一部分が変わっただけの特定の化合物についてHMG-CoA還元酵素阻害活性を有する蓋然性が高いと理解することがあるものと認められる。 しかし,甲2の実施例1~23や上記認定の特定の化合物には,スルホンアミド構造を有する化合物は含まれていない。証拠(乙65)及び弁論の全趣旨によると,化学物質がわずかな構造変化で作用の変化を来す可能性があることは,技術常識であるから,甲2の一般式(I)で示される極めて多数の化合物全部について,実施例1~23や上記認定の特定の化合物と同程度又はそれを上回るHMG-CoA還元酵素阻害活性を有すると期待できるわけではなく,HMG-CoA還元酵素阻害活性が失われることも考えられる。 したがって,甲2から,甲2の一般式(I)で示される極めて多数の化合物全部について,技術的裏付けがあると理解できるとはいえないのであって,原告らの上記主張は,前記aの判断を左右するものではない。 仮に,甲2に相違点(1-ⅰ)に係る構成が記載されていると評価できたとしても,前記(2)のとおり,甲1発明の化合物である「
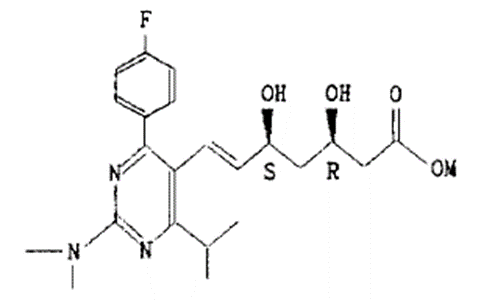
(M=Na)の化合物」である「(3R,5S)-[E]-7-[4-(4-フルオロフェニル)-6-(1-メチルエチル)-2-(ジメチルアミノ)ピリミジン-5-イル]-3,5-ジヒドロキシ-6-ヘプテン酸ナトリウム」は,甲1の実施例1b)の生成物であり,HMG-CoA還元酵素阻害活性を有するものであって,甲1の一般式Iで示される化合物に包含され,また,甲1には,甲1の式Iのピリミジン環の2位の置換基R2の選択肢として「-N(R8)2」が記載され,さらに,R8の選択肢として「メチル基」が記載されているものの,R8の選択肢としては「アルキルスルホニル基」は記載されていない。 そうすると,甲1には,甲1発明の化合物のピリミジン環の2位の「ジメチルアミノ基」を,甲1の式Iの選択肢には含まれない「-N(CH3)(SO2R’)」に置き換える動機付けとなる記載があるとはいえない。 b(a) コレステロールの大部分は肝臓で合成されること,HMG-CoA還元酵素がコレステロールの生合成を触媒すること,HMG-CoA還元酵素阻害剤がコレステロールの生合成を阻害することは,本件優先日当時,当業者の技術常識であったと認められる(甲7,10,11,14)。 本件優先日当時,「種々のHMGR(HMG-CoA還元酵素)阻害剤の組織(肝)選択性の性質及び有無の両方に関して文献上でかなりの議論がなされて」おり(甲7),また,「HMG-CoA還元酵素阻害薬に含まれるロバスタチンとシンバスタチンがイヌにおいて高用量で白内障を引き起こす可能性がある」という所見があった(甲24)。 そうすると,副作用を考慮して,大部分のコレステロールが合成される肝臓に対して選択性が高いHMG-CoA還元酵素阻害剤を得ようとすることは,本件優先日当時の技術的課題として当業者が認識し得るものであったといえる。 (b) 甲7(弁論の全趣旨によると,平成3年1月1日に発行されたものと認められる。)には,ロバスタチン,プラバスタチンなどのHMG-CoA還元酵素阻害剤となる化合物について,「組織選択性は主に薬剤の相対的親油性による影響を受け,相対的に親水性の高い化合物が高い肝選択性を示す」との仮説を検討したところ,「肝臓と他の組織とで選択性が等しくなる『交差』点は,CLOGP≒2」であり,「これより下の場合,化合物は肝臓に選択的で,これより上の場合は末梢組織に選択的となる」ことが記載されている。また,甲20には,プラバスタチン,ロバスタチン,メバスタチン及びシンバスタチンという四つのHMG-CoA還元酵素阻害剤の親油性(logP)を測定し,ヘキサヒドロナフタレン環の6位にメチル基を有するロバスタチンやシンバスタチンよりも,水酸基を有するプラバスタチンのlogPの値が低いこと,そのような物理化学的特性により,プラバスタチンが肝臓外の細胞によって余り効率的に取り込まれないといえるであろうことが記載されている。 以上の甲7及び甲20の記載からすると,HMG-CoA還元酵素阻害剤において,相対的に親水性の高い化合物が,肝選択性を高める可能性があることが示唆されているといえるから,副作用を考慮して,肝臓に対して選択性が高いHMG-CoA還元酵素阻害剤を得るために,HMG-CoA還元酵素阻害活性を示す化合物を,親水性という指標で評価し,親水性の高い(logPが2以下の)化合物を選択するという動機は本件優先日当時の当業者が認識できたものといえる。 (c) しかし,一方で,ピリジン及びピリミジン置換3,5-ジヒドロキシ-6-ヘプテン酸のラクトンのHMG-CoA還元酵素阻害活性について記載された甲16には,中央の芳香族環の6位における嵩高の親油性の置換基が合成HMG-CoA還元酵素阻害剤の生物活性に大きく寄与することが記載されるとともに,以下の構造式(以下「甲16構造式」という。)「
Y=表Ⅱの番号2a~2qにおいてCH,同番号2t~2wにおいてN)」において,中央の芳香環(ピリミジン環)の2,4及び6位(R1,R2及びR3)における置換が強力な生物活性をもたらすこと,2位(R1)にイソプロピル基を導入すれば生物活性は最大になること,4位(R2)の4-クロロフェニル及び4-フルオロフェニル置換の類縁体が同等に強力な阻害剤となること,6位(R3)の置換は最適な生物活性のために最も重要で,嵩高のアルキル基の導入又はフェニル部分の導入によって力価の顕著な上昇を得ることができることが記載されている。 ここで,甲1発明の化合物は,ジヒドロキシヘプテン酸のラクトン体ではなく,ジヒドロキシヘプテン酸のナトリウム塩ではあるものの,甲16構造式において,「2:A-B=(E)-CH=CH」であって,R1にイソプロピル基が導入され,かつ,R2が4-フルオロフェニル置換されたものに相当するから,甲16の記載に接した当業者であれば,甲16構造式におけるR3に相当する,甲1発明の化合物のピリミジン環の2位の「ジメチルアミノ基」の部分に,嵩高の親油性の置換基,特に,嵩高のアルキル基又はフェニル部分を導入することにより力価の顕著な上昇を期待できると認識するといえる。 そうすると,たとえ,本件優先日当時,副作用を考慮して,HMG-CoA還元酵素阻害活性を示す化合物であって,より親水性の高い化合物を選択するという動機があったとしても,その一方で,甲1発明の化合物においては,そのピリミジン環の2位の「ジメチルアミノ基」部分に,嵩高の親油性の置換基,特に,嵩高のアルキル基あるいはフェニル部分を導入することにより力価の顕著な上昇を期待できると当業者は認識したといえるから,甲1発明の化合物のピリミジン環の2位の「ジメチルアミノ基」を,嵩高の親油性の置換基とはせずに,より親水性の高い置換基とすることの動機付けが,本件優先日当時の当業者にあったとはいえない。 (d) また,甲9及び甲60には,メチル基よりも親水性の高い基として,メチルスルホニル基(-SO2CH3)以外の基も相当数記載されており,たとえ,甲1発明の化合物のピリミジン環の2位のジメチルアミノ基を,より親水性の高い置換基とすることの動機が本件優先日当時の当業者にあったとしても,本件優先日当時の技術常識からでは,その一方のメチル基を,メチルスルホニル基という特定の基とすることの動機までもが本件優先日当時の当業者にあったとはいえない。 さらに,甲1発明の化合物のピリミジン環の2位のジメチルアミノ基の一方のメチル基をメチルスルホニル基とする動機付けがないことと同様の理由により,甲1発明の化合物のピリミジン環の2位のジメチルアミノ基の一方のメチル基を,メチルスルホニル基を除くアルキルスルホニル基(エチルスルホニル基,プロピルスルホニル基等)とする動機付けもない。 (e) したがって,仮に,甲2に相違点(1-ⅰ)に係る構成が記載されていると評価できたとしても,甲1発明の化合物のピリミジン環の2位のジメチルアミノ基を「-N(CH3)(SO2R’)」に置き換えることの動機付けがあったとはいえないのであって,甲1発明において相違点(1-ⅰ)に係る構成を採用することの動機付けがあったとはいえない。 なお,原告らは,審決は,サポート要件の判断では,「コレステロールの生成を抑制する」医薬品となり得る程度に「優れたHMG-CoA還元酵素阻害活性」を有する化合物又はその化合物を有効成分として含むHMG-CoA還元酵素阻害剤を提供することという課題を設定して判断している一方で,進歩性の動機付けの判断は,課題の基準である「コレステロールの生成を抑制する」医薬品となり得る程度を超える「甲1発明化合物のHMG-CoA還元酵素阻害活性が現状維持されること」という基準を設定し,判断しているから,このようなダブルスタンダードでサポート要件と動機付けを判断することは妥当ではないと主張する。 上記主張のうち,審決のサポート要件についての上記判断が正しいことは,後記4のとおりである。これに対し,進歩性については,既に判示したとおり,甲2に相違点(1-ⅰ)に係る構成が記載されておらず,また,仮に甲2に相違点(1-ⅰ)に係る構成が記載されていると評価できたとしても,相違点(1-ⅰ)の構成を採用する動機付けがあったとはいえないことから,容易に発明をすることができたとはいえないと判断されるのであって,原告らが主張するような基準を設定して判断しているものではないから,原告らが主張するような矛盾が生ずることはない。 (カ) 以上のとおり,甲1発明において,相違点(1-i)の構成を採用することができたとはいえない。 イ 小括 そうすると,相違点(1-ⅱ)について検討するまでもなく,当業者が,甲1発明に甲2発明を組み合わせることにより,本件発明1を容易に発明をすることができたとは認められない。 また,本件発明2,5及び9~11の化合物は本件発明1に包含されるものであるところ,本件発明1につき,当業者が容易に発明をすることができたとはいえない以上,本件発明1を更に限定した本件発明2,5及び9~11についても,当業者が容易に発明をすることができたということはできない。 さらに,本件発明12のHMG-CoA還元酵素阻害剤は,本件発明1の化合物を有効成分として含有するHMG-CoA還元酵素阻害剤であるところ,本件発明1につき,当業者が容易に発明をすることができたとはいえない以上,本件発明12についても,当業者が容易に発明をすることができたということはできない。したがって,本件発明1,2,5及び9~12は,いずれも甲1発明に甲2発明を組み合わせることにより,容易に発明をすることができたとは認められず,原告ら主張の取消事由1は理由がない。 |
3 検討
ア 主引用発明としての適格性
米国におけるリード化合物理論を当事者が主張していたことから判断したもの。本判決は、「技術分野」のみを考慮要素としている。
本判決抜粋
|
このような進歩性の判断に際し,本願発明と対比すべき同条1項各号所定の発明(以下「主引用発明」といい,後記「副引用発明」と併せて「引用発明」という。)は,通常,本願発明と技術分野が関連し,当該技術分野における当業者が検討対象とする範囲内のものから選択されるところ, 前記2(2)のとおり,本件発明は,コレステロール生合成の律速酵素である3-ヒドロキシ-3-メチルグルタリルコエンザイムA(HMG-CoA)還元酵素を特異的に阻害し,コレステロールの合成を抑制することにより,高コレステロール血症,高リポタンパク血症,更にはアテローム性動脈硬化症の治療に有効な,HMG-CoA還元酵素阻害剤に関するものであり,前記(2)アのとおり,甲1発明も,コレステロール生合成における律速酵素である3-ヒドロキシ-3-メチルグルタリル補酵素A(HMG-CoA)の拮抗阻害剤であって,血中コレステロールレベルを降下させる過脂肪蛋白血症処置剤及び抗アテローム性動脈硬化剤に関するものであるから,本件発明と技術分野を共通にし,本件発明の属する技術分野の当業者が検討対象とする範囲内のものであるといえる。 |
米国の裁判例は、下記のように基本的には主引例に限定はないと考えている。
参考:Eisai Co. Ltd. v. Dr. Reddy’s Labs., Ltd., 533 F. 3d 1353 (Fed. Cir. 2008).
|
クレームされた化合物は、最も近い先行技術のリード化合物を修正してクレームされた化合物を得る理由がなく、かつ先行技術がリード化合物を修正すればその有利な特性が害されると教示している場合には、自明でなかったはずである。いかなる公知の化合物もそこから開始すべき何らかの理由がありかつそれを修正してクレームされた化合物を得る何らかの理由があるならば、リード化合物となることができる。 構造上の類似性に基づく自明性は、当業者がある公知の化合物(リード化合物)を選択しこれを特定のやり方で修正してクレームされた化合物を得るようにさせる何らかの動機を特定することによって、証明され得る。 |
日本における議論は、下記のとおり後知恵排除を主張する者が多い。
(ア)主引例適格性の議論肯定
塚原朋一(「特許の進歩性判断の構造について」知的財産法の新しい流れ422頁、青林書院)
| 従来発明A’は本件発明Aの存在を前提にして初めて入手し得た発明であるから、本件発明Aがなくても、従来発明A’を見つけることができたことの容易性を基礎づける根拠を提示することが必要である。 |
高橋淳(「進歩性の判断II」知財プリズム105号23頁)
| 事後分析的な後知恵の判断を回避するためには、対象となる発明を認識しないという想定の下で引用例の選択が容易であったことを論証する必要がある |
(イ)主引例適格性の議論否定
末吉剛(http://d.hatena.ne.jp/oneflewover/20131026/1382800369)
| しかし、日本の判断枠組みの下では、主引用例適格性を改めて持ち出す必要はないように思います。不適切な(つまり、発想の方向が異なる)主引用発明しか見つけられなかったのであれば、たとえ構成が本願発明と近接していても、通常、動機づけは否定できます。 |
前田健・小林純子(パテント2010 Vol63 No.7、119頁)
| なお,本件発明を念頭に引用例の探索を網羅的に行うことは,進歩性判断における後知恵排除とは矛盾しない。進歩性判断における後知恵排除とは進歩性判断のすべての段階について求められるものではない。厳密に後知恵排除を追究するという考えを徹底すれば,引用発明の認定の際にも,本件発明を念頭におかずに探索すべきことになる。しかし,そのような探索は実際には不可能であるので,引用発明の認定の際には後知恵を許す。一方,相違点についての判断(容易想到性の判断)の段階では厳しく後知恵の排除を要求する。このような明確な区分をおくことによって,手法として明快かつ合理的なものになるのである。 |
イ 相違点を埋める論理付けとして「発明」を要するか
不要と思われる。判決も「甲2発明」との言葉を殊更取り上げたわけではなく、「相違点1-ⅰの構成」といった文言と同視している。
本判決抜粋
|
したがって,引用発明として主張された発明が「刊行物に記載された発明」であって,当該刊行物に化合物が一般式の形式で記載され,当該一般式が膨大な数の選択肢を有する場合には,特定の選択肢に係る技術的思想を積極的あるいは優先的に選択すべき事情がない限り,当該特定の選択肢に係る具体的な技術的思想を抽出することはできず,これを引用発明と認定することはできないと認めるのが相当である。 この理は,本願発明と主引用発明との間の相違点に対応する他の同条1項3号所定の「刊行物に記載された発明」(以下「副引用発明」という。)があり,主引用発明に副引用発明を適用することにより本願発明を容易に発明をすることができたかどうかを判断する場合において,刊行物から副引用発明を認定するときも,同様である。 |
(ア)発明とそれ以外とを区別すべきでないとする説
前田健・小林純子(前掲)
| ある技術思想を相違点を埋めるために参照している時,それが単なる副引用発明ではなく技術常識であるとされると,審査・審判段階においては新たな拒絶理由にはならず(35),裁判段階においては,審理範囲違反にならないとされることがある。しかしながら,「技術常識」と呼ぶことによって,新たな拒絶理由通知の必要性や審理範囲違反の問題を回避しているにすぎないという側面は否定できない。このように単なる副引用発明と技術常識(周知・慣用技術)とを区別して扱うことがなぜ許されるのかが問われなければならない。 |
*なお、「発明か、相違点に係る構成か」との議論からは脱線するが、「容易の容易」の議論においても、副引用発明と技術常識とが区別されている。
(イ)発明の認定とそれ以外とを区別する説
実務一般。
ウ 副引用発明の認定の問題としたことの是非
本判決抜粋
| したがって,甲2から,ピリミジン環の2位の基を「-N(CH3)(SO2R’)」とするという技術的思想を抽出し得ると評価することはできないのであって,甲2には,相違点(1-ⅰ)に係る構成が記載されているとはいえず,甲1発明に甲2発明を組み合わせることにより,本件発明の相違点(1-ⅰ)に係る構成とすることはできない。 |
(ア)進歩性の水準
本判決は、相違点に係る構成の記載がないとして、動機づけを検討するまでもなく門前払いしているから、複数の選択肢が挙げられている化学分野の発明の進歩性の基準を下げるものであると思われる(たとえ相違点の構成を選ぶ動機づけの記載が別文献ないし技術常識として存在しても、そもそも相違点の構成が開示されていなければ発明に至らない)。
(イ)選択発明理論との整合
どこまでの「上位概念」であれば発明として認定され、どこからが「発明」として認められないのか。主引例に基づく新規性判断の場合で考えると、発明として認定された場合、進歩性は原則否定され、発明として認定されなければ進歩性が肯定されるという両極端な結果となる。選択肢が膨大であることのみを理由として上位概念発明に基づく新規性を否定することは乱暴である。
これに対し、引用発明の認定として考えず、動機づけの問題として捉えれば、選択発明理論と整合的に理解できる。
参考:知財高裁平成29年 6月14日(平28(行ケ)10037号)
| 特許に係る発明が,先行の公知文献に記載された発明にその下位概念として包含されるときは,当該発明は,先行の公知となった文献に具体的に開示されておらず,かつ,先行の公知文献に記載された発明と比較して顕著な特有の効果,すなわち先行の公知文献に記載された発明によって奏される効果とは異質の効果,又は同質の効果であるが際立って優れた効果を奏する場合を除き,特許性を有しないものと解するのが相当である |
(ウ)複数の文献から発明を認定することの是非
複数の文献から発明を認定することと、膨大な選択肢から発明を認定することとは利益状況が似ており、否定説と親和性があるように思われる(いずれも「技術的思想」の開示の有無という同一の考慮要素である)。
a 否定
知財高判平成19 年9 月26 日・平成18 年(行ケ)第10174 号
| 29 条2 項を適用する場合における同条1 項3 号にいう『…頒布された刊行物に記載された発明』とするためには,引用発明とする技術が(2つの刊行物に)それぞれ開示されていることが必要であり,一方に存在しない技術を他方で補って併せて一つの引用発明とすることは,特段の事情がない限り,許されない |
エ 動機づけは副引例に存在してもいいのか
本判決は、下記の通り甲1に動機づけが存在するかを判断する一方、甲2に動機づけがあるか否かは判断していない。
しかし、本判決は単に甲1に動機づけ記載がないことを積極的に認定したにすぎず、動機づけは当業者にとってあればよいとの従前の理解と異ならない。
本判決抜粋
| そうすると,甲1には,甲1発明の化合物のピリミジン環の2位の「ジメチルアミノ基」を,甲1の式Iの選択肢には含まれない「-N(CH3)(SO2R’)」に置き換える動機付けとなる記載があるとはいえない。 |
オ 類似裁判例
清水元判事は従前から同様の判決をしている。
知財高裁平成28年10月12日(平27(行ケ)10212号) *清水コート
| ところで,発明とは,自然法則を利用した技術思想の創作であり,自然法則上の制約からも,また,発明者の創作意図としても,一まとまりの技術事項として構成されるものであるから,明細書などの同一の文献の中に,発明の各構成要素が複数の候補から選択できるものとして記載されているような場合であっても,その選択肢の組合せの全ての類型が,当然に,当該文献に発明の構成として開示されているものと解することはできない。 |
以上
(文責)弁護士・弁理士 森下 梓